
بیماریهای نئوپلاستیک و مدیریت درمان سرطان در بارداری
بیماریهای نئوپلاستیک و مدیریت درمان سرطان در بارداری
نئوپلاسم هاى دستگاه تولید مثل
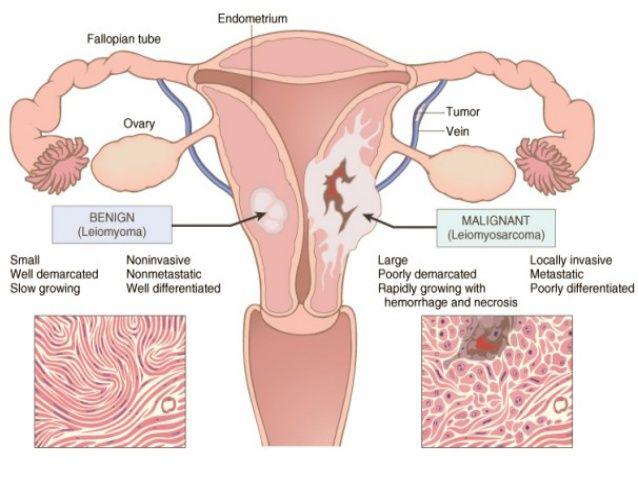
نئوپلاسم هاى خوش خیم شایع هستند و شامل مایوما،نئوپلاسم هاى تخمدان،پولیپ سرویكس ،میباشند
كانسر در این ارگانها باعث افزایش عوارض باردارى مى گردد
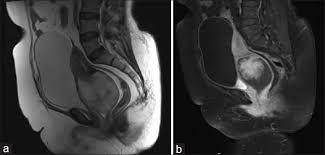
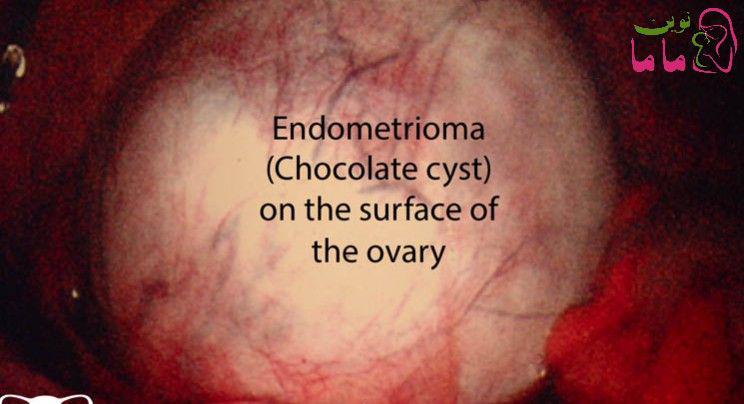
شایع ترین سرطان بدخیم دستگاه تولید مثل در زمان باردارى ،سرویكس (تصویر 2-63)٧٠٪ و بعد از آن تخمدان با ٢٣٪میباشد
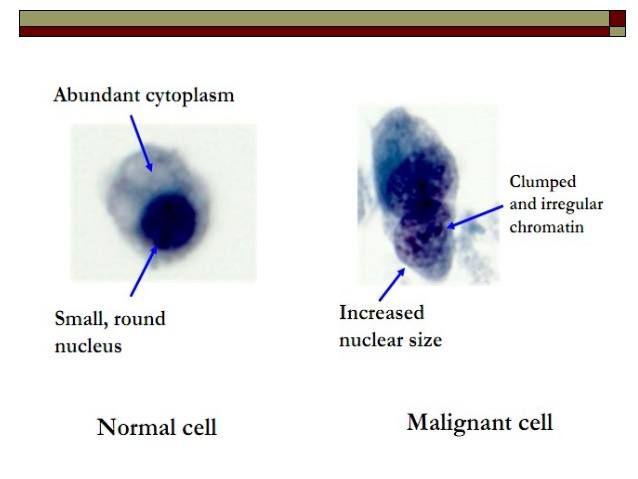
سرویکس
1, پولیپ سرویكس
پولیپ رشد استروماى اندوسرویكس،، كه بوسیله اپیتلیوم پوشیده شده است
معمولا، بصورت تك ،قرمز،كشیده و گوشتى با سایزهاى مختلف كه از كانال اندوسرویكس به سمت بیرون امتداد یافته است
معمولا خوش خیم است
اغلب خونریزى كند
اغلب منشأ نتیجه پاپ اسمیر؛
Atypical Glandular cell of Undetermined Significance-AGUS
باشد
با برداشتن و ارزیابى هیستولوژى پولیپ
٠/٥ درصد،دیسپلازى
٠/١درصد،تغییرات بدخیمى
دیده میشود
مطالعات كمى براى راهنمایى درمان و ارائه پولیپ در باردارى،در اختیار داریم
ضایعات بدون علامت،ممكن است باقى گذاشته شود تا در زمان زایمان یا بعد از زایمان، حذف شود
برداشتن پولیپ و ارزیابى هیستولوژى
شامل:
شك به بدخیمى
خونریزى آزاردهنده
مناسب میباشد
براى این كار،پولیپ توسط رینگ گرفته شده،چرخانده میشود…تا به پایه پولیپ برسیم،جایى كه عروق در آن قراردارد…با ادامه چرخش پایه پولیپ باریكتر شده و نهایتا از جا كنده میشود
…میتوان از Monsel paste كه همان ferric subsulfate است،استفاده نمود و با فشار بر روى ریشه پدیكل پولیپ ،جهت هموستاز،گذاشت
…ساقه ضخیم پولیپ گاهأ احتیاج به برش جراحى و بستن ،پیدا میكند
2, اپى تلیال نئوپلازى CIN
باردارى یك شرایط مناسب براى غربالگرى سرویكال اینترا اپى تلیال نئوپلازىCIN،بخصوص در خانمهایى كه تحت مراقبت نبوده اند،میباشد
بر روى برگه پاپ اسمیر،حتما باردارى قید شود،زیرا تغییرات فیزیولوژیك ایجاد شده در سرویكس،تفسیر را متفاوت خواهد كرد
بعضى از تغییرات ایجاد شده شامل:
سلولهاى decidual
واكنش Arias-Stella ،البته به میزان كمتر
بتدریج ،،تغییرات بصورت،،هایپرپلازى غدد اندوسرویكس میگردد كه تشخیص آن از atypical گلاندولار سل حقیقى ،مشكل میباشد
گایدلاین غربالگرى در سال ٢٠١٢ (كه براى باردارى هم قابل انجام است) توسط ASCCP،به روز گردید
دستوالعمل شامل:
احتیاج به غربالگرى تا سن ٢١ نیست
سایتولوژى به تنهایى،هر سه سال ،در افراد بین ٢٩-٢١سال
بالاى ٣٠ سال
سایتولوژى وHPV با هم،كوتست
Co-testing ،هر پنج سال
یا سایتولوژى به تنهایى هر سه سال
شرایط پر خطر براى CIN
عفونت با HIV
شرایط كاهش ایمنى فرد
فرادى كه در دوره جنینى در معرض DES قرار گرفته اند
براى خانمهایى كه HIV دارند،شروع غربالگرى سرویكس،در یكسال اول بعد از تشخیص HIV ،میباشد
ویروس پاپیلوماى انسانىHPV
این ویروس ،اپیتلیوم سرویكس را درگیر میكند
در اغلب موارد عفونت پاك میشود
اما در تعداد كمى،ویروس ممكن است به رشد خود ادامه داده،premalignant یا malignant شود
وقوع HPV در خانم باردار١٥٪ است
بیش از صد نوع سروتایپ دارد،چندسروتایپ آن مثل ١٦ و ١٨ همراه با CIN و سرطان تهاجمى میباشد
انجامHPV تایپینگ ،تست اولیه به تنهایى در خانمهاى بالاى ٢٥ سال میباشد،در صورت وجود سروتایپ ١٦ ،١٨ ارزیابى كلپوسكوپیك باید انجام شود
سروتایپ ٦،١١مرتبط با زگیل تناسلى خوش خیم مادرى میباشد
عفونت مادرزادى HPV ،حاصل از انتقال عمودى(یعنى مادر به جنین یا نوزاد)از طریقtransient skin colonization ،،،نادر میباشد
اما با وجود زگیل تناسلی درناحیه؛پرینئال،ولوار،لارینژیال،كانژانكتیوال؛در زمان تولد یا در عرض ٣-١سال بعد از تولد ،میتواند بر اثر برخورد با سروتیپ HPV مادرى بوجود آید
نكته مهم: سزارین باعث كاهش لارینجیال پاپیلوماتوز نوزادى نمیگردد
ارتباط واضح بین عفونتHPV و سرویكال نئوپلازى ،منجر به ساخته شدن سه نوع واكسن گردیده است
این واكسنها در طول باردارى تزریق نمیگردد ولى با شیردهى مشكلى ندارد
سرطان مهاجم سرویكس
كارسینوم سلول سنگفرشی ٧٥ درصد از تمام سرطانهای سرویكس را شامل میشود و آدنوكارسینوم سرویكس عامل ٢٠ تا ٢٥ درصد است.
سرطانها ممكن است به اشكال زیر دیده شوند:
توده اگزوفیتیك یا اندوفیتیك ،توده پولیپوئید ،بافت پاپیلری یا سرویكس بشكه ای شكل ،اولسراسیون یا بافت نكروتیك
ممكن است ترشح آبكی ،چركی ،بدبو یا خونی وجود داشته باشد.
درصورت وجود ضایعات مشكوك نمونه برداری با فورسپس Tischlerضرورت دارد.
٧٠ درصد سرطانهای تشخیص داده شده در دوران حاملگی در مرحله I قرار دارند.
نكته مهم این است كه اندوراسیون قاعده رباط پهن كه از خصوصیات گسترش تومور به خارج سرویكس است ممكن است در نتیجه نرم شدن نواحی سرویكس ،پاراسرویكس و پارامتر در اثر حاملگی وضوح كمتری داشته باشد.
از MRI بدون ماده حاجب گادولینیوم و ترجیحا بعد از سه ماهه اول برای تایید در گیری مجاری ادراری و گره های لنفاوی می توان استفاده كرد.
تدابیر درمانی و پیش آگهی:
مرحله IA1 مرحله تهاجم میكروسكوپی نامیده میشود و ضایعاتی را توصیف میكند كه عمیقترین تهاجم آنها ٣ میلی متر و وسیعترین گستره جانبی ٧ میلی متر یا كمتر است .
ادامه حاملگی و زایمان واژینال رویكرد بی خطری در نظر گرفته میشود و درمان قطعی ٦ هفته بعد زایمان صورت می گیرد.
سرطان مهاجم واقعی به درمان نسبتا فوری نیاز دارد.اكثر متخصصان درمان فوری در طول نیمه اول حاملگی را توصیه میكنند اما این امر به به تصمیم گیری بیمار در مورد ادامه یا عدم ادامه بارداری بستگی دارد .
اگر بیماری در نیمه دوم حاملگی تشخیص داده شود اكثریت توافق دارند كه حاملگی به صورت بی خطر نه تنها تا كسب قابلیت حیات جنین بلكه تا كسب بلوغ ریه جنین ادامه یابد.
در مطالعات انجام شده به تعویق انداختن درمان در زنان فاقد ضایعات حجیم منطقی است و می توان مرحله بندی با لنفادكتومی لاپاراسكوپی صورت گیرد و در صورت رد متاستاز درمان به تاخیر انداخته شود.
در یك متاآنالیز شیمی درمانی نئوادجوان با مشتقات پلاتینیوم امید بخش بوده است.
اكثر زنان مبتلا به ضایعات مرحله I و مرحله IIA ابتدایی هیستركتومی رادیكال همراه لنفادنكتومی لگن درمان ارجح محسوب میشود قبل ٢٠ هفته هیستركتومی در حالی كه جنین داخل رحم است انجام میشود بعد ٢٠ هفته ابتدا هیستروتومی انجام میشود.
پرتو درمانی در مراحل پیشرفته سرطان صورت میگیرد.در مراحل اولیه حاملگی از پرتوتابی با منبع خارجی استفاده می شود و اگر سقط خود به خود رخ ندهد كورتاژ صورت میگیرد.در سه ماهه دوم حاملگی ممكن است سقط به سرعت رخ ندهد و هیستروتومی در یك چهارم موارد ضرورت یابد.
در زنان حامله و غیر حامله مبتلا به سرطان مهاجم سرویكس میزان بقا به أزا هر مرحله یكسان سرطان مشابه است
زایمان:
درمواردی كه ضایعات حجیم یا شكننده هستند ممكن است خونریزی شدید در اثر زایمان واژینال به وجود بیاید.همچنین عود در محل اسكار اپیزیاتومی به علت كاشته شدن سلول های تومور در محل اپیزیاتومی گزارش شده است.
زایمان سزارین ارجح است.
حاملگی بعد از تراكلكتومی رادیكال:
در جریان عمل واژینال تیپیك سرویكس درسطح سوراخ داخلی آمپوته میشود و یك سوچور سركلاژ دائمی برای حمایت حاملگی های آتی در ناحیه ایسم قرار داده میشودو ناحیه ایسم رحم مجدد به واژن اتصال داده میشود. به دلیل وجود سركلاژ دائمی از انسزیون كلاسیك سزارین استفاده میشود.
لیومیوم ها ( فیبروئید)
فیبروئید هم نامیده میشوند. تومورهای خوش خیم عضله صاف هستند. میزان بروز این ضایعات در دوران حاملگی تقریبا ٢ درصد است و میزان بروز آنها بستگی به كاربرد سونوگرافی روتین و ویژگیهای جمعیت بستگی دارد.
شروع لیومیوم در زنان سیاهپوست در سه ماهه اول حاملگی در بیشترین حد و زنان سفید پوست در كمترین حد است.
مقاله درمان فیبروم در یائسگی را مطالعه کنید
محل میوم متغیر است ممكن است به صورت ساب موكوزال ،ساب سروزال یا اینترامورال به وجود آیند.
این تومورها باشیوع كمتر در سرویكس یا رباط پهن إیجاد می شوند.
بعضی از این تومورها حالت پارازیتی پیدا میكنند و خون آنها از ساختمان های مجاور مثل امنتوم پرعروق فراهم می شود.
در مورد نادری به نام لیومیوماتوز منتشر صفاقی تعداد بسیار زیادی تومور خوش خیم عضله صاف در موقعیت زیر صفاقی با نمایی مشابه كارسینوماتوز منتشر تظاهر می یابند.
این تومورها احتمالا از تحریك استروژنی سلول های چند مركزی مزانشیمی زیر سلومی وتبدیل آنها به سلول های عضله صاف ناشی می شوند .
این تومورها در اغلب موارد بعد از حاملگی پسرفت می كنند.
اثر تحریك حاملگی بر رشد میوم غیر قابل پیش بینی است وممكن است قابل توجه باشد.
نحوه پاسخ تومورها متفاوت است واندازه این تومورها در حاملگی ممكن است افزایش یا كاهش پیدا كند و یا بدون تغییر بماند.
میومها به ویژه در دوران حاملگی ممكن است با سایر توده های آدنكسی اشتباه شوند و تصویر برداری سونوگرافی ضروری است.
در زنانی كه یافته های سونوگرافی انها واضح نیستند ممكن است بعد از سه ماهه اول حاملگی MRI ضرورت پیدا كند.
مقاله غربالگری در 3 ماهه اول بارداری را اینجا بخوانید
در مورد میوم ها بعد تشخیص نیازی به سونوگرافی سریال نیست مگر اینكه احتمال بروز عوارض پیش بینی شود.
علایم:
اكثرا بدون علامت هستند. ممكن است احساس فشار و یا درد حاد یا مزمن إیجاد شود.میوم بزرگ اغلب نیاز به بستری برای درد دارد.
در صورت درد مزمن ناشی از اندازه بزرگ تومور میتوان از داروهای آنالژزیك غیر ناركوتیك استفاده كرد.
دربرخی موارد رشد میوم ها از حد توان خونرسانی فراتر می رود و انفاركت هموراژیك رخ میدهد كه به این حالت دژنرسانس قرمز یا گوشتی گفته می شود.از نظر بالینی درد یا حساسیت حاد كانوتی شكم وجود دارد وگاهی اوقات تب خفیف و لكوسیتوز دیده می شود.

افزایش دو برابری سزارین در دنیا
در چنین مواردی ممكن است افتراق دژنرسانس تومور از آپاندیسیت ،دكولمان جفت،سنگ حالب یا پیلونفریت دشوار باشد.
سونوگرافی ممكن است كمك كننده باشد اما نظارت دقیق ضروری است چون تشخیص میوم انفاركته با رد كردن سایر احتمالات تشخیصی صورت میگیرد . در بعضی از زنان التهاب تومور سبب تحریك لیبر می شود.
درمان میوم دژنره با استفاده از داروهای آنالژزیك صورت میگیرد در اكثر مواقع علایم در عرض چند روز برطرف میشود درموارد شدید نظارت دقیق برای رد كردن علل سپتیك ضروری است. در موارد بسیار انتخابی میومكتومی نتایج خوبی به همراه دارد تقریبا در نیمی از زنان جراحی به دلیل درد صورت گرفته بود.
بعضی از مواقع میوم های پایه دار زیر سروزی تورشن پیدا میكنند و متعاقبا دچار نكروز دردناك میشوند.در این موارد می توان از لاپاراسكوپی یا لاپاراتومی برای بستن پایه تومور و برداشتن تومور نكروتیك استفاده كرد.
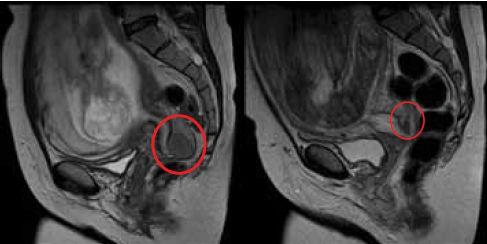
عوارض حاملگی
لیبر پره ترم ، دكولمان جفت ،پرزنتاسیون غیر طبیعی جنین،توقف لیبر ،زایمان سزارین و خونریزی بعد زایمان
در یك مطالعه بروز دكولمان جفت و نمایش بریچ چهار برابر ،بروز خونریزی سه ماهه اول و اختلال عملكرد لیبر دو برابر و میزان سزارین ٦ برابر بیشتر بوده است .
در یك مطالعه دیگر گزارش كردند كه خطر سقط سه ماهه دوم ٨ برابر افزایش می یابد.
عامل مهم در تعیین موربیدیتی حاملگی تعداد میوم ،اندازه ومحل آن هستند.به ویژه اگر جفت در مجاورت میوم باشد یا روی آن لانه گزینی كرده باشد خطر سقط ،لیبر پره ترم ،دكولمان جفت و خونریزی بعد زایمان افزایش میابد.
میوم های خلف جفت همراه با محدودیت رشد جنینی است.
تومورهای واقع در سرویكس یا سگمان تحتانی رحم ممكن است سبب توقف لیبر شوند .علی رغم این عوارض میزان زایمان واژینال در زنانی كه اندازه میوم آنها ١٠ سانت یا بیشتر است به ٧٠ درصد میرسد.
در صورتی كه میوم آشكارا مجرای زایمان را مسدود نكرده باشد آزمون لیبر مجاز است.
اگر سزارین اندیكاسیون پیدا كند میوم عموما به حال خود رها میشود مگر اینكه باعث خونریزی غیر قابل مهار شده باشد.
انجام هیستركتومی هنگام سزارین ممكن است از نظر تكنیكی دشوار باشد چون تومور سبب جابه جایی طرفی حالب می شود.
خونریزی ناشی ازمیوم در دوران حاملگی در اثر عوامل متعددی ممكن است إیجاد شود.خونریزی به ویژه در اثر سقط ،لیبرپره ترم،پلاسنتا پرویا و دكولمان شایع است.
در موارد نادر خونریزی در اثر میوم زیر مخاطی كه به داخل سرویكس یا واژن پرولاپس پیدا كرده است رخ میدهد.اگرچه خونریزی شدید یا مداوم نیازمند مداخله سریع است میتوان ساقه میوم را در نزدیكی ترم از طریق واژینال مسدود كرد تا از كنده شدن تومور در حین زایمان جلوگیری شود.
خوشبختانه میوم ها به ندرت عفونی میشوند ،اگر تومور بلافاصله در مجاورت محل لانه گزینی جفت قرار داشته باشد،این حالت با بیشترین شیوع در دوره بعد زایمان رخ میدهد.
همچنین میوم ها ممكن است به علت سقط عفونی یا سوراخ شدن میوم در اثر ورود سوند، دیلاتور یا كورت آلوده شوند.
ملاحظات در زمان بارداری
علی رغم شیوع بالآی میوم مشخص نیست به جز ارتباط احتمالی میوم با سقط. آیا این ضایعات با عث كاهش باروری یا ناباروری می شوند یا خیر
میوم زیر مخاطی تأثیر چشمگیر بر باروری دارند ومیومكتومی هیستروسكوپیك سبب كاهش میزان ناباروری وسقط زود هنگام در این زنان می شود.
میوم های مرتبط با ناباروری و محل های دیگر ممكن است برای اكسزیون تومور لاپاراسكوپی یا لاپاراتومی ضرورت یابد.
بعد میومكتومی هم قبل وهم طَی لیبر نگرانی پارگی رحم وجود دارد كه اگر رزكسیون تومور منجر به إیجاد شكاف به داخل حفره اندومتر یا مجاورت آن شود سزارین قبل شروع لیبر انجام می شود.
از آمبولیزاسیون شریان رحمی نیر برای درمان ناباروری یا علایم میوم استفاده شده است اما تأثیر آن كمتر از جراحی است.
در زنانی كه با آمبولیزاسیون شریان رحمی درمان میشوند میزان سقط خود به خود زایمان سزارین وخونریزی بعد زایمان افزایش میابد.آمبولیزاسیون میوم درزنانی كه قصد دارند بعدا حامله شوند كنتر اندیكاسیون نسبی دارد.
در نهایت ulipristal كه یك تعدیل كننده رسپتورهای پروژسترونی است برای پسرفت میوم استفاده شده است و موارد متعدد حاملگی های موفق بدون رشد تومور گزارش شده است.
کانسر پستان
ریت کانسر پستان بطور شایع بین سنین۴۰ تا ۸۰ سال اقزایش دارد اما بعلت شیوع بالای آن در زنان جوان نیز شایع میباشد

در یک نمونه بیماران ۱۱.۸میلیون تولد انسیدانس حدود ۱۵۰۰۰ بوده است ودرزنانی که در سنین بالاتر بچه دار میشوندقطعاشیوع سرطان همزمان پستان افزایش میابد در سوئد و ودانمارک افزایش سن بارداری مسئول افزایش درصد ریسک کانسر پستان شناخته شده است.
زنان دارای سابقه خانوادگی سرطان پستان بویژه دارای موتاسیون BRCA1&BRCA2با احتمال بیشتری در دوران حاملگی دچار بدخیمیهای پستان میشوند
گر چه خطردراز مدت ابتلا به سرطان پستان در افراد حامل این جهشها قطعا افزایش میابد ولی عامل پاریتی این خطر را تعدیل میکند طوری که در زنان مسن تر از ۴۰زایمان کرده بسیار کمتر از نولی پور ۴۰ ساله مبتلا میشوند ولی سقط القایی و شیر دهی تغییری در افزایش ریسک نمیدهند بلکه حتی در زنان BRCA1شیردهی اثر محافظتی نیز دارد( نهBRCA2)در موردتماس باDESاختلاف نظر وجود دارد
دستوالعمل غربالگری سرطان پستان
تشخیص سرطان پستان
بیش از ۹۰ در صدزنان حامله ماس قابل لمس دارند و بیش از ۸۰ در صدتوسط خود بیمار کشف میشوند برسی بالینی و تشخیص و درمان در زنان حامله مبتلا به سرطان پستان معمولا با تاخیر صورت میگیرد که بعلت تغییرات بافت پستان حین بارداری و مخفی شدن توده ها میباشد
روند ارزیابی زنان حامله با ماس پستان نباید تفاوت با غیر باردار داشته باشد و هر نوع توده مشکوک و قابل لمس باید تحت بیوپسی و اکسیژن قرار گیرد
اگر برای افتراق توده سالید و کیستیک تصویر برداری لازم باشد سونو حساسیت و ویژگی بالایی دارد
در صورتی ماموگرافی اندیکاسیون داشته باشد خطر تابش اشعه به جنین با فیلد محافظ قابل چشم پوشی میباشد ولی بعلت دنس برست در حاملگی منفی کاذب بالای۳۵ تا۴۰ در صد داریم اگر تصمیم برای بیوپسی قطعی نباشد از MRIنیز استفاده میکنیم
ضایعات پستان به دو دسته ساده یا کامپلیکه تقسیم بندی شده است. کیست ساده نیازی به در مان یا تدابیر خاص ندارد و در صورت علامت دار شدن اسپیره میشوند در سونوگرافی کیستهای
کامپلیکه اکو های داخلی غیر قابل افتراق از توده سالید دیده میشود که ابتدا اسپیره میشوند و اگر برطرف نشوند اقدام به core need le
درمان
پس از تشخیص سرطان پستان برسی محدود مناطق شایع متاستاز با گرافی سینه وسونوی کبد وMRI اسکلتی انجام میشود
وظیفه درمان بعهده تیم تخصصی شامل متخصص مامائی و جراح پستان و اونکولوژیست طبی است و باید قبل درمان در مورد تمایل بیمار به ادامه یا ختم حاملگی مشورت شود ختم حاملگی تاثیری در بهبودندارد و کلا درمان در حاملگی مشابه غیر حامله است ولی شیمی و جراحی تا تریمسر دوم و رادیو تراپی تا ختم حاملگی به تاخیر می افتد
درمان جراحی ممکنست قطعی بوده ودر غیاب متاستاز اکسیژن وسیع یا ماستکتومی توتال یا مدیفیه استفاده کرد .staging با بیوپسی گره لنفاویsentinelو لنفوسیتوگرافی با تکنزیوم۹۹ بی خطر است ولی رنگهایایزو سولفان و متیلن بلو گروه C حاملگی هستند .باز سازی پستان پس از زایمان انجام می شود
ولی در یک مطالعه ۱۰ خانم حامله بلافاصله پس از ماستکتومی ترمیم پستان شدند و نتیجه خوب داشتند

شیمی درمانی در سرطان پستان هم نود مثبت وهم منفی داده میشود ودر زنان پره منو پوز بقا پیشرفت دارد برای نود مثبت شیمی درمانی چند دارویی شروع میشود اگر منتظر زایمان قریب الوقوع نباشیم سیکلو فسفامید دوکسور بیسین وسیسپلاتین اغلب استفاده میشوند اگر انتراسیکلین ها مانند دوکسور بیسین استفاده شودبعلت مسمومیت قلبی اکو قلب مادر توصیه میشود
ایمونو تراپی برای برای سرطان پستان به روش رایجی تبدیل شده است تراستوز ماب نوعی انتی بادی منو کلونال است علیه گیرنده HER2 neu در یک سوم سرطان های مهاجم پستان دیده میشوند عمل میکند ودر بیشتر مواقع درمان کمکی در مراحل ابتدایی تومورهای حاویHER2 بکار میرود در حاملگی استفاده نمیشود و این دارو باعث سقط و نارسایی کلیه جنین والیگو و پره ترم میشود در مدت درمان و تا ۶ ماه بعد جلو گیری از بارداری توصیه میشود
پیش آگهی
اثر حاملگی بر سرطان پستان و پروگنوز پیچیده است شکی نداریم که سرطان پستان در زنان جوانتر تهاجمی تر است ولی اکثر مطالعات نشان میدهند که بقای بیمار در حاملگی تفاوتی با غیر حامله ندارد ولی اکثرا نتیجه گیری شده که در حاملگی مراحل پیشرفته تر بیماری دیده میشود و لحاذا پیشاگهی در حاملگی ضعیفتر است
۶۰ در صد زنان حامله سرطان پستان در گیری نود دارند ولی در مقایسه مرحله به مرحله بقای ۵ساله مشابه است بیشتر بودن شیوع مراحل پیشرفته پیشاگهی را تضعیف می کند
حاملگی بعد سرطان پستان
بعد از درمان سرطان پستان بعضا نازایی ناشی از شیمی درمانی داریم و لی نتایج طولانی تاثیر نامطلوب حاملگی بدنبال سرطان پستان را نشان نداده ولی از آنجا که موارد عود بدنبال درمان شایع تر هستند بتاخیر انداختن ۲تا۳سال حاملگی جهت نظارت بر درمان معقول بنظر میرسد روشهای هورمونی کنتراسپشن ممنوع ولی ایودی مسی روش مناسب میباشد
بطور کلی زنان بدنبال درمان سرطان پستان پیامد خوب دارند ولی زنان بعد مصرف تاموکسیفن تا دو ماه نباید حامله شوند
سرطان تیرویید
نودهای تیروئید قابل لمس در۴تا۷ درصد جامعه دیتکت شده که ده درصد مالین هستند ونودهای کلینیکی با سونو و ارزیابی Tsh و fT4ارزیابی میشوندFAN در نود مشکوک اندیکاسیون دارد
ختم حاملگی ضروری نیست ودرمان اولیه تیروئید کتومی توتال در سه ماهه دوم و سپس جایگزینی با لوتیروکسین میباشد
اکثر سرطانهای تیروئید تمایز خوب دارند و بتاخیر انداختن جراحی پیامد بیماری را تغییر نمی دهد
در بعضی از بدخیمیهای تیروئید ید رادیو اکتیوبصورت اولیه یا بعد جراحی تجویز میشود که البته در حاملگی و شیردهی هر دو کنتراندیکه میباشد
فاصله بین شیر دهی و تخریب تیروئید با ید رادیو اکتیو سه ماه است و برای حاملگی مجدد پس از درمان با ید۱۳۱ شش ماه تا یکسال میباشد

لنفومها
بیماری هوچکین
احتمالا از سلولهای Bمنشا میگیرند و با دیدن سلولهای رید اشتنبرگ قابل افتراق از سایر لنفومهاست
هوچکین شایعترین نوع لنفوم بدخیم زنان سنین باروری است و۷۰۹ میلیون تولد انسیدانس یک در۱۲.۴۰۰ بوده است
در بیش از ۷۰ در صد موارد هوچکین بزرگی بدون درد گره های لنفاوی بالای دیافراگم وجود دارد تقریبا یک سوم بیماران علائم تب تعریق شبانه احساس کسالت کاهش وزن و خارش دارند و تشخیص با برسی هی ستو پاتولوژی گره های لنفاوی در گیر صورت میگیرد
STAGING
از سیستمAnn Arborبرای مرحله بندی استفاده میشود
حاملگی برسیهای رادیو گرافیک را برای استیجینگ محدود میکند ولی حداقل اقدامات تشخیصی شاملCxR و سونو ی شکمی و MRI و Bone Marrow بیوپسی
MRI
ابزاری عالی برای گره های سینه ای و پارائورتی شکمی است
درمان افراد غیر باردار شیمی درمانی است ولی در خانم باردار مراحل ابتدایی در سه ماهه اول:نظارت تا بعدهفته۱۲ شیمی تک دارویی با این بلاستین تا سه ماهه دوم و سپس ختم و شیمی چند دارویی یا پرتو برای مناطق منفرد اگزیلری و گردنی
شیمی درمانی برای مراحل پیشرفته تر بیماری صرف نظر از سن حاملگی توصیه میشود قبل از هفته 20 سقط درمانی و اگر ختم ندهیم سه ماهه دوم بعد از درمان با وین بلاستین از درمان چند دارویی استفاده میکنیم بعد ازسه ماهه اول برای درمان مراحل بسیار پیشرفته از دوکسوروبیسین بلئومایسین وین بلاستین داکار بازین تجویز میشوند و بعد از زایمان پرتو درمانی اضافه میشود
نکته مهم :زنان هوچکین ابتلا بالای ترومبوامبولی وریدی عفونت و سپسیس دارند درمان فعال انتی نئوپلازی هم ابتلا به عفونت را افزایش میدهد
پیش اگهی کلی لنفوم هجکین خوب است و میزان بقا به بیش از 70 % میرسد و حاملگی تاثیر نامطلوبی در بقا ندارد
درمان ها هم تاثیری در پیامد های نامطلوب جنینی ندارند در نیمی از زنان پس از پایان شیمی درمانی قاعدگی های طبیعی از سرگرفته شده عوارض دراز مدت لنفوم :لوسمی ثانویه در افرادی که شیمی درمانی شده اند سرطان ثانویه ی پستان در پرتو درمانی انفارکتوس میوکارد فیبروز ریوی هیپوتیروئیدی و سرکوب مغز استخوان لنفومهای نان هوجکین اگر چه لنفوم های غیر هوجکین معمولا از نوع سرطان تومور های سلول B هستند ، ممکن است از نوع نئوپلاسمهای سلول T یا سلول نچرال کیلر است . این لنفوم ها با عفونت های ویروسی در ارتباط هستند و افزایش چشمگیری یافته اند یکی از دلایل ابتلا 5 تا 10 % افراد HIV مثبت به لنفوم است دیگر ویروس ها اپشتن بار ویروس هپاتیت C و ویروس هرپس انسانی هستند نان هوجکین در حاملگی شایع نیست .
درمان:
در سه ماهه اول به جز موارد ابتدایی و ارام ختم حاملگی و شیمی چند دارویی
انواع کمتر تهاجمی یا تحت نظر یا تحت درمان موقت با پرتودرمانی کانونی ناحیه فوق دیافراگم قرار میگیرند و درمان کامل پس از شروع سه ماهه دوم اغاز میشود اگر بعد از سه ماهه اول تشخیص داده شود شیمی و ایمونو تراپی با ریتوکسیماب انجام میشود و این درمان ها ناحنجاری مادرزادی نداشته اند .
لنفوم بورکیت ، نوعی تومور تهاجمی سلول B است که با عفونتت ویروس اپشتن بار در ارتباط است پیش اگهی ضعیف و درمان چند دارویی است .
لوسمی ها
کلا یا از بافتهای لنفویید یا مغز استخوان منشا میگیرند و حاد یا مزمن هستند واگر چه لوسمی های بزرگسالان بعد از ۴۰ سالگی شایعترند ولی در زنان جوان هم جز شایعترین بدخیمیها بشمار میایند حدود یک در۴۰۰۰۰ حاملگی گزارش شده اند لوسمی مزمن در زنان جوان نا شایع است
لوسمی حاد ابنرمالیتی سلولهای خون محیطی(WBC)و سلولهای بلاست در گردش میشود
تشخیص بیوپسی مغز استخوان (Bone Marrow)
با کمو تراپی چند دارویی رمیشن در حاملگی شایع شده ولی قبلامرگ و میر حدود۱۰۰ در صد بوده
بعلت تراتوژنیسته بالای شیمی درمانی سقط در مراحل اولیه حاملگی مد نظر قرار میگیرد
در درمان لوسمی حاد از اسید رتینویک که عامل تراتوژن قوی سندرم اسید رتینویک استفاده نمیشود
درمان مشابه غیر بارداری است و بعد شیمی القایی پیشگیری از عود با پیوند سلول بنیادی
عفونت و خونریزی از عوارض مهمی هستند که در بیماران فعال مشکل آفرین هستند و پره ترم و مرده زایی هم افزایش میابد
ملا نوم بدخیم
اکثرا از پوست و خالهای موجود قبل و ملانوسیتهای تولید پیگمان منشاء میگیرند
هر گونه تغییر شکل برجستگی سطحی تغییر رنگ خارش خونریزی و زخمی شدن احتمال ملانوم و فورا بیوپسی میشود در افراد سفید پوست شایعترند ودر یک مطالعه جدید یکی از شایعترین بدخیمیهای دوران بارداری میباشدواز ۳صدمتا ۲.۸مورد در۱۰۰۰ تولد زنده گزارش شده
متاستاز به جفت و جنین میدهند و بعد زایمان جفت باید برای پاتولوژی ارسال شود
مرحله بندی بالینی است
مرحله اول بدون نود قابل لمس
مرحله دوم نود های قابل لمس دارند
سوم متاستاز دور دست
در مرحله اول ضخامت عامل پیشگویی بقا میباشد
طبقه بندی Clarkبر اساس عمق نفوذ به اپیدرم و..پنج سطح دارد
معیارBreslowعلاوه برعمق تهاجم ضخامت و اندازه تومور نیزسنجش میشود
درمان شامل رزکشن موضعی وسیع و گاهی دیسکسیون گسترده گره های لنفاوی منطقه ای
الگوریتمی برای بیماران حامله مطرح شده که شاملرزکشن تومور اولیه با بیحسی موضعی و بیوپسی گره لنفاویsenttinelتا بعد زایمان به تعویق میافتد
در حاملگی شیمی درمانی یا ایمنوتراپی پروفیلاکتیک پرهیز میشود ولی اگر براساس مرحله لازم باشد استفاده میشود
در متاستاز دور دست رویکرد تسکینی داریم
اخیرا نقش گیرتده بتا استروژنی در ملانوم بعنوان یک هدف در درمانهای آینده ند نظر میباشد
مرحله بالینی بیماری پیشگویی بقا میدهند تهاجم عمیق ودر گیری نود منطقه ای بدترین پیشاگهی دارند
بعلت خطر عود بالا ۳تا۵ سال پیشگیری از حاملگی توصیه میشود قرص جلو گیری فاقد آثار نا مطلوب میباشد
سرطانهای دستگاه گوارش
سرطان کولورکتال
بدخیمیهای کولو رکتال سومین سرطان شایع در تمام گروههای سنی زنان میباشد ولی در حاملگی بندرت بوجود میآید چون زیر ۴۰ سال نا شایع است حدود یک در ۱۵۰۰۰۰۰ تولد
در حاملگی بیشتررکتوم در گیر است
شایعترین علائم درد شکمی اتساع شکم تهوع و استفراغ یبوست و خونریزی از رکتوم میباشد و چون در حاملگی این علائم شایع است تشخیص به تعویق میافتد
تشخیص با معاینه انگشتی رکتوم تست خون مخفی وسیگمویدسکوپی یا کولونسکوپسی
درمان مشابه غیر بارداری است در نیمه اول بارداری هیسترکتومی اجباری نیست ودر مراحل آخر میتوان درمان را تا بلوغ ریه به تاخیر انداخت و بهتر است زایمان غیر واژینال باشد
CEA
اندازه گیری انتی ژن برای مانیتوریگ بیماری مفید است
سایر سرطانهای گوارشی :سرطان معده بندرت در حاملگی هست و اکثرا درژاپن گزارش شده اند تشخیص با اندوسکوپی است.
درمان كانسر در باردارى
1_جراحى
روشهاى جراحى جهت،تشخیص،staging یا درمان میباشد
خوشبختانه اغلب روشهاى جراحى با دستگاه تولید مثل تداخل نداشته و براحتى توسط مادر و جنین تحمل میگردد
گرچه چه بصورت كلاسیك،بسیارى از عملهاى جراحى بعد از هفته ١٤-١٢باردارى انجام میشود تا شانس سقط به حداقل برسد،،،،،ولى الزامى نیست
در هر زمانیكه لازم باشد،،در هر سن جنینى و بر اساس سلامتى مادر،،جراحى انجام گردد
باردارى و سرطان هر دو ریسك فاكتورهاى ترومبوآمبولى وریدىVTEمیباشند
در یك مطالعه در سال ٢٠١٦ توسط Bleau،ریسك بالاتر VTEدر خانمهاى باردار مبتلا به میلوئید لوكمیا،هاجكین،كانسر CX و تخمدان در مقایسه با افراد باردار بدون سرطان ،گزارش كردید.البته در افراد مبتلا به سرطان مغز یا تیرویید و ملانوما و لوكمیاى لنفویید،افزایش ریسك دیده نشد.
بنابراین گفته میشود گایدلاینهاى موجود فاقد توصیه هاى خاص براى بیماران سرطانى تحت عمل در دوران باردارى میباشد.پس،بر اساس پیچیدگى جراحى انتخابى براى مادر باردار ،، از هپارینLMWهمراه با جوارب هاى الاستیك و/یا فشار متناوب نوماتیك،میتوان استفاده كرد
2_ اسكن هاى تشخیصى
سونوگرافى
روش ارجح ،در باردارى است
اگرچه بر اساسACOG 2017،اغلب روشهاى رادیوگرافى تشخیصى به میزان خیلى كم،أشعه داشته و نباید تأخیر در انجام آنها،درصورتیكه تأثیر مستقیم بر روى شروع درمان داشته باشند،صورت پذیرد
MRI چیست
در سرتاسر باردارى كاملا بى خطر میباشد
اما تاخیر در انجام آن تا پایان سه ماهه اول باردارى ممكن است باعث كاهش ریسك هاى بالقوه گردد
گادلینیوم نباید در سه ماهه اول استفاده گردد و باید در ماههاى بعد ،فقط،زمانیكه فوائد آن ،خیلى مهمتر از
ریسك استفاده از آن باشد،استفاده گردد
روشCT
بخاطر أشعه یونیزه و روشهاى وابسته به دوز كمتر انتخاب مى گردد(فصل٤٦ ص ٩٠٦)
بنابراین زمانى از CT در باردارى استفاده میشود كه براى تشخیص موارد حاد؛مثل آمبولى ریوى،انسداد روده و كلیه،حوادث حاد نورولوژیك؛باشد
براىenhanceكردن CTممكن است كانتراست خوراكى یا تزریقى اضافه گردد كه احتیاج به قطع شیر مادر ندارد
بعضى از انواع رادیوایزوتوپ نسبتا در باردارى بى خطر میباشد
3_ رادیوتراپى
رادیوتراپى باعث در معرض قرار گرفتن قابل توجه جنین بر اساس،دوز أشعه،محل تومور،سایز زمینه أشعه،سن حاملگى،میگردد
اثرات منفى بالقوه شامل ؛جنین مالفورم،ناتوانى ذهنى ،محدودیت رشد،نازایى،كارسینوژن؛میباشد
رادیوتراپى دو هفته بعد از لقاح ،منجر به آسیب كروموزومى و مرگ آمبریو،میگردد
آسیب پذیرترین مرحله بعدى،بین هفته ٨-٢ باردارى،ارگانوژنز میباشد و باعث مالفورمیشن میگردد،در این زمان ،میزان أشعه بالاتر از دوز آستانه یعنىGy،٠/٢-٠/١میباشد
بین هفته ٢٥-٨ بخصوص،CNSجنین ،آسیب پذیر میباشد
آستانه
دوز آستانه أشعه براى ناتوانى ذهنى
در هفته١٥-٨ جنینى ٠/٠٦
در هفته٢٥-١٦ جنینى٠/٢٥Gy
میباشد
بعد از هفته ٢٥ جنینى،حساسیت كمتر شده،،،،،اما هیچ سن جنینى براى رادیوتراپى،بى خطر نیست
بنابراین،رادیوتراپى به شكم مادر باردارممنوع است
در بعضى از كانسرهاى سر و گردن،رادیوتراپى به محل سوپرادیافراگماتیك (البته با محافظ شكمى جنین )میتواند نسبتأ بى خطر باشد

4_ كموتراپى
داروهاى مختلف ضد سرطان،براى اولین بار یا بعنوان درمان تكمیلى، در دوران باردارى استفاده میشوند
اگرچه شیمى درمانى،اغلب باعث بهبود نتایج سلامتى مادر در طولانى مدت میگردد،بسیارى براى استفاده از آن بى میل هستند
نگرانى براى جنین؛ جهت مالفورمیشن،محدودیت رشد،ناتوانى ذهنى،شانس سرطان در آینده در دوران بچگى میباشد
ریسك بصورت اولیه بر اساس سن جنین در زمان شیمى درمانى میباشد.اغلب داروها در سه ماهه اول(در طى ارگانوژنز)مضر میباشند
در یك بررسى،١٤٪ مالفورمیشن هاى ماژور بخاطر مصرف داروهاى سایتوتوكسیك در سه ماهه اول ،بوده است
بعد از سه ماهه اول،اغلب داروهاى آنتى نئوپلاستیك ،بدون اثر فورى و قابل مشاهده مضر،بر روى جنین میباشند
…همچنین در این دوره اثرات موتاژنیك دیررس،محدود میباشد
اگر چه همیشه عملى نیست،بعضى پیشنهاد میكنند،كموتراپى سه هفته قبل از موعد زایمان،متوقف شود،زیرا نوتروپنى یا پان سایتوپنى ممكن است باعث افزایش ریسك عفونت یا خونریزى در مادر شود
نگرانى دیگر كلیرانس كبدى و كلیوى نوزاد براى متابولیت هاى شیمى درمانى محدود میباشد،به همین دلیل اكثر داروهاى شیمى درمانى سایتوتوكسیك، در زمان شیردهى ممنوع میباشد
5_ مولكولار تراپى
داروهاى تحریك كننده خونسازى،بصورت شایع در كانسر استفاده میشوند،بعضى از اینها شامل فاكتورهاى. تحریك كننده كلنى گرانولوسایتها مثل
Filgrastim(Neupogen)
Pegfilgrastim(Neulasta)
اگر در باردارى لازم شود،اطلاعات كمى براى بى خطرى این داروها وجود دارد
البتهErythropoietin alfa(procrit)باعث تحریك RBC میگردد، بصورت Case report گزارش شده در باردارى بى خطر است.البته فشار خون مادر یك ریسك بالقوه است

6_ تارگت تراپى
دو تیپ اصلى دارند
Monoclonal Abs
Small molecule inhibitors
هر دو،عمل آنزیمهاى اختصاصى و مولكولهاى درگیر در رشد سلولهاى كانسرى را بلاك میكنند
این داروها براى درمان لیست زیادى از كانسرها،طراحى شده اند،اكثرا بوسیله FDA در گروهDقرار گرفته و داده ها در باردارى و شیردهى محدود میباشد
خیلى از این داروها،نشانگاه تیروزینkinase میباشند كه آنزیم مهمى در تنظیم راههاى درگیر براى تقسیم سلولى و تمایز سلولى و آپوپتوز میباشد…استفاده در سه ماهه اول،مسمومیت آمبریو یا تراتوژنسیتى به همراه دارد…
بنابراین،از این گروه دارو،تركیبات تارگت در باردارى تنها زمانى استفاده میگردد كه سود بالقوه آن توجیه كننده ریسك خطر براى جنین باشد
از داروهاى دیگر،هرسپتین میباشد
Monoclonal antibody transtuzumab
Herceptin.
…باعث مهار گیرنده HER2
Human Epidermal growth factor
Receptor type 2
میگردد(این گیرنده ها ،در بعضى از انواع. كانسر BX خود را نشان میدهد)
…اگرچه هرسپتین تراتوژن نیست،استفاده از آن در سه ماهه دوم و سوم با اولیگوهیدرامینوس میباشد كه بنظر قابل برگشت با توقف دارو میباشد
…بخاطر اطلاعات كم از مهار كننده هاى دیگر HER2 در باردارى استفاده نمیگردد
بارورى و باردارى بعد از درمان كانسر
بارورى ممكن است بعد از شیمى درمانى و رادیوتراپى كاهش یابد
مشاوره قبل از شروع درمان انجام میگردد،گایدلاینى هم در این رابطه موجود میباشد
قبل از شروع درمان،فریز جنین یا تخمك در مواردى كه نگهدارى بارورى مدنظر باشد،انجام میشود
جابجایى جراحى تخمدان ها میتواند در زمان رادیوتراپى به لگن ،مد نظر باشد،بدین منظور تخمدان ها و عروق خونرسان آنها را از لگن جابجا كرده و به دیواره جانبى شكم،بفاصله٤-٣ سانت بالاى ناف،فیكس میكنند
…در یك مطالعه،نگهدارى عملكرد تخمدان در ٩٤-٦٤٪ موارد،بر اساس نوع رادیوتراپى،حفظ شده بود
…گرچه این جابجایى،ممكن است احتیاج، به گرفتن تخمك از طریق شكم در زمانیكه تصمیم به IVF در فرد داریم،پیدا كند
سركوب تخمدان با آگونیست GnRH،سودمند نیست
در حال حاظر،فریز بافت تخمدان در دست تحقیق است
شواهد پیشنهاد میكنند كه شیمى درمانى یا رادیوتراپى در زمان بچگى یا نوجوانى،تغییر قابل توجهى در افزایش ریسك آنومالیهاى مادرزادى یا بیماریهاى ژنتیكى در فرزندان این افراد ندارد
…بعضى مطالعات،افزایش مختصر در آمار سزارین و زایمان زودرس را نشان میدهد
…بعضى مطالعات،افزایش آمار سزارین و زایمان زودرس را در بچه هایى كه میزان دوز درمانیشان به اندازه بزرگسالان بوده است،نشان میدهد
قابل توجه است كه پرتودرمانى لگن و شكم،اثر بیشترى بر Neonatal out come دارد
…اثرات مضر شامل افزایش سقط،وزن كم زمان تولد،still birth،تولد نارس،میباشد
…پرتودرمانى ممكن است باعث كاهش پتانسیل تولید مثل بوسیله كوچك كردن حجم رحم و نازك كردن ضخامت اندومتر و ضعیف شدن جریان خون رحم شود
…اثرات بیشتر با رادیوتراپى مستقیم رحم و سن كمتر در زمان رادیوتراپى میباشد
مطلب مهم،بسیارى از افراد بازمانده از درمان كانسر،با ART باردار شده،كه بنوبه خود باعث افزایش ریسك هاى حاملگى میگردد

متاستاز جفت
تومورها بندرت به جفت متاستاز میدهند،شایعترین آن ملانوم بدخیم،لوكمیا،لیمفوما و كانسر BX میباشد
جفت باید در همه افراد مبتلا به سرطان، براى پاتولوژى فرستاده شود،زیرا سلولهاى سرطانى معمولا در فضاى بین ویلاى جفتى دیده میشود
…اگر چه متاستاز به جنین نادر است
منبع بارداری وزایمان ویلیامز
نوشته وگردآوری راضیه فرقانی













نظرات شما